�v���X�����[�X
���l�s����w
�|����Ɍ������n��W�I�|�P�b�g�̔����|
�T�v
�@�����w�������i�����j�����@�\�Ȋw�����Z���^�[�G�s�W�F�l�e�B�N�X���䌤���`�[���i���������j�̔~�����j�`�[�����[�_�[�i���������A���n��^���p�N����͊�Ճ��j�b�g�㋉�������j�A�e�n�����������i���������A��������Ȋw�����Z���^�[�Ɖu�튯�`�������`�[���������j�A�������Ȋw�����Z���^�[�P�~�J���Q�m�~�N�X�����O���[�v�̈ɓ������q����nj������i������ȑ�w�����Ȋw�������j�A���l�s����w��w�@������Ȋw�����ȍ\���G�s�Q�m���Ȋw�������̏�����������̋��������O���[�v�́A�����̃^�C�v�̂���זE�ō��������Ă���^���p�N��GAS41[1]���A�㐬��`���[2]�i�G�s�W�F�l�e�B�b�N���j��S���q�X�g��H3�^���p�N���̃A�Z�`�����C��[3]��F�����A����̈�`�q�̔���������������d�g�݂����܂����B
�@�{�������ʂɂ��AGAS41�����������Ă��鑽��ނ̂���זE�̑��B��}���鐧�䕪�q�̍����I�ȊJ�������҂���܂��B
�@�q�g���͂��߂Ƃ���^�j�זE[4]�̃Q�m��DNA�̓k�N���I�\�[��[5]�Ƃ����\�����`�����ċÏk���Ă���A�G�s�Q�m��[2]�͂ǂ̈�`�q�̃k�N���I�\�[�������̓]��[6]�ɐ旧���ĉ����ق������𐧌䂵�Ă��܂��B
�@����A���������O���[�v�͍\�������w�E�����w�E�זE�����w�̎�@��GAS41�̍\���Ƌ@�\����͂��܂����B���̌��ʁAGAS41�^���p�N�����A�q�X�g��H3�́uN���[[7]�v�ƁuN���[���琔����14�Ԗڂ܂���27�Ԗڂ̃��V���c��[8]�̃A�Z�`�����C���v�����ꂼ��قȂ�|�P�b�g��p���ĔF�����A�k�N���I�\�[����H2A.Z�Ƃ����q�X�g���̕ώ�^���p�N���̓����𑣐i���邱�ƂŁA����̈�`�q��]�ʂ��₷������d�g�݂����炩�ɂȂ�܂����B
�@�{�����́A�Ȋw�G���wProceedings of the National Academy of Sciences�iPNAS�j�x�I�����C���Łi10��16���̏T�j�Ɍf�ڂ���܂��B
[�摜1]https://user.pr-automation.jp/simg/1706/77803/600_207_20231016130219652cb5cb12280.jpg
GAS41���G�s�Q�m���C���̈ʒu��[���琔����d�g�݂̉�
�w�i
�@�㐬��`���̓G�s�Q�m������]�ʂ����`�q�̎��Ɨʂ̐���Ɋւ�邱�Ƃ��m���Ă��܂��B�������m���Ă���㐬��`���̒��ł��q�X�g���̃A�Z�`�����C���́A���זE�����̂��ꂼ��̍זE��ɓ��ٓI�ɔ������Ă����`�q�̓]�ʂ������������ŏd�v�ƍl�����Ă��܂��B�ߔN�A�k�N���I�\�[�������̃q�X�g���ɂ����郊�V���c��̃A�Z�`�������ǂ̂悤�ȏ����œ`�d���Ĉ�`�q�̓]�ʂ����������邩�̎d�g�݂�A�q�X�g���̓���̃��V���c��̃A�Z�`�������G�s�Q�m������̈�`�q�]�ʂ̂ǂ̔����f�ߒ������������邩�̎d�g�݂Ȃǂ���������Ă��܂���1�A2�j�B
�@�q�X�g���̃A�Z�`�����C������`�q�]�ʂ̊������������N�����d�g�݂ɂ͕����̌o�H������܂��B�d�v�Ȑ���o�H�Ƃ��āA�A�Z�`�������ꂽ�q�X�g���̎�ނ�V���c��̈ʒu���������ĔF������u�ǂݎ�v�^���p�N�����ւ��o�H���m���Ă��܂��B�q�X�g���̃A�Z�`�����C���ɑ��ẮA�u�����h���C��[9]��YEATS�h���C��[1]�����^���p�N������v�ȁu�ǂݎ�v�^���p�N���ł���A�זE���ł����̃^���p�N���̔��������i����Ƃ���≊�ǂȂǂ̎����ɂȂ��邱�Ƃ��m���Ă��Ă��܂��B
�@�u�����h���C�����q�X�g���̃A�Z�`�����C����F������d�g�݂ɂ��Ă͉�͂��i��ł���A����̃u�����h���C�������^���p�N���̋@�\��I��I�ɑj�Q���鉻�����̊J���₻��𗘗p��������@�\�̌������i�߂��Ă��Ă��܂���3�A4�j�B���̈���AYEATS�h���C�����q�X�g���̃A�Z�`�����C����F������d�g�݂ɂ��Ă͕s���ȓ_�������AYEATS�h���C���ɑ���j�Q�܂̊J�����x��Ă���ł����B
�@�����ŋ��������O���[�v�́A�q�g��4��ޑ��݂���YEATS�h���C���ܗL�^���p�N���̂����A�������̈��ł����P���i����������j�זE[10]�ň�`�q������������GAS41�ɒ��ڂ��܂����BGAS41�́A�^�j�����̎�Ԃŕۑ����ꂽ�N���}�`��[5]�̍\���𐧌䂷��^���p�N�������̂̍\�������̈�ł���A�N���}�`���̍\����ω������邱�Ƃň�`�q�̓]�ʂ����������܂��BGAS41�̈�`�q���P���זE�����łȂ��A�݂����̂���A��������A����������A�������x����̍זE�ʼnߏ蔭���������A�זE����GAS41��`�q�̔�������߂�Ƃ��̂悤�Ȕ�������y���ł��邱�Ƃ��ߔN�m���Ă��܂��BGAS41�ɂ�锭�����́AGAS41��YEATS�h���C�����q�X�g���̃A�Z�`�����C����F�����邱�ƂƊ֘A���Ă��܂����A���̔F�����ǂ̂悤�Ȏd�g�݂ɂ���ĒS���Ă���̂��ɂ��Ă͕s���ȓ_������܂����B�����Ŗ{�����ł́AGAS41��YEATS�h���C������Ăǂ̂悤�Ƀq�X�g���̓���̃A�Z�`������Ԃ�F�����čזE���ŋ@�\����̂��̎d�g�݂̉𖾂�ڎw���܂����B
��1�j2023�N7��17���v���X�����[�X�u��`�q�����𐧌䂷��G�s�Q�m���̕����Ɠ]�ʁv
https://www.riken.jp/press/2023/20230717_1/
��2�j2020�N11��26���v���X�����[�X�u�G�s�Q�m���̐�������]�ʂ̕������v
https://www.riken.jp/press/2020/20201126_1/
��3�j2018�N8��8���v���X�����[�X�u�w����G�s�Q�m���x�����o����V��@�v
https://www.riken.jp/press/2018/20180808_2/
��4�j2023�N10��3���v���X�����[�X�u��`�q����������������X�[�p�[�G���n���T�[�̍Ē�`�v
https://www.riken.jp/press/2023/20231003_1/
������@�Ɛ���
�@���������O���[�v�͏��߂ɁAGAS41��YEATS�h���C�����q�X�g���̂ǂ̂悤�ȃA�Z�`������Ԃ�F������̂��ɂ��āA�q�X�g���̎�ށAN���[�e�C���ɂ�����A�Z�`�����C���̈ʒu�AN���[�e�C���̒�����ς��Đ����w�I�ɔ�r�������܂����B���̌��ʁAGAS41��YEATS�h���C���̓q�X�g��H3��N���[���琔����14�Ԗڂ̃��V���c��̃A�Z�`�����iK14ac�j�ƍł������������邱�ƁA����ɂ��̌����ɂ̓q�X�g��H3��N���[1�`6�Ԗڂ܂ł̃A�~�m�_�c��s���Ȃ��Ƃ�������܂����B�ʏ�A�u�ǂݎ�v�^���p�N���́A����̉��w�C�����܂ރA�~�m�_�c��Ƃ��̑O��̐��J���̎c��̃A�~�m�_�z���F�����܂��B����̃f�[�^�́AGAS41��YEATS�h���C�����q�X�g��H3�́uN���[�v�ƁuK14ac�v�Ƃ������ꂽ2�J�������炩�̕��@�ŔF������d�g�݂�����Ă��邱�Ƃ��������܂����B
�@�����Ŏ��ɁAK14ac���܂ރq�X�g��H3��N���[�e�C���̈��GAS41��YEATS�h���C���Ƃ̕����̂̌�����X���ō\����͂��܂����B���̌��ʁA���V���A�Z�`�������u�ǂށv�@�\������GAS41��YEATS�h���C���͊m���ɃA�Z�`���������q�X�g��H3�e�C����K14ac�Ƃ��̎��ӂ̃A�~�m�_�z��Ɍ������Ă��܂����i�}1�A���[�̃p�l���j�B���̌����́AYEATS�h���C�����`������F�����P�[�W�ƌĂ��|�P�b�g�ɂ���ĒS���Ă��܂��B
[�摜2]https://user.pr-automation.jp/simg/1706/77803/600_168_20231016130221652cb5cdc0285.jpg
�}1�@GAS41���q�X�g��H3��N���[�e�C����F������2��ނ̎d�g��
�����̃p�l���F����3���̃p�l���̂����̒����̃p�l����GAS41��YEATS�h���C���ƃq�X�g��H3�y�v�`�h�Ƃ̕����̂̌����\���̑S�̂���
�@�@�@�@�@�@�@���A���̍��E�̃p�l����2�ӏ��̌����ꏊ�̊g��}�������Ă���B�q�X�g��H3�̃y�v�`�h�����F�̃X�e�B�b�N�ŁAGAS41��
�@�@�@�@�@�@�@YEATS�h���C�����x�[�W���ł��ꂼ�ꎦ���B�e�c��̈ʒu�́A�A�~�m�_�̎�ށi1�����\�L�j�Ǝc��̈ʒu�i�����j�̃��x��
�@�@�@�@�@�@�@�Ŏ����B
�E�[�̃p�l���FGAS41��YEATS�h���C���̕��q�\�ʃ��f���B���q�\�ʂ̑a�����̓x������ΐF���甒�F�̃O���f�[�V�����Ŏ����B��蔒�F��
�@�@�@�@�@�@���q�\�ʂ����a���I�ł���B�q�X�g��H3��N���[�e�C����1�Ԗڂ̃A���j���iA1�j����3�Ԗڂ̃X���I�j���iT3�j�܂ł̃A�~
�@�@�@�@�@�@�m�_�c�GAS41��YEATS�h���C���̂��ڂ݁iH3NT�|�P�b�g�j�ɂ���ĔF������Ă���B
�@�����GAS41��YEATS�h���C���́A���̖F�����P�[�W�ɂ�錋�����ʂ��痣�ꂽ�ꏊ�ŁA��L�Ƃ͕ʂ̃q�X�g��H3�e�C����N���[�̈�ƌ������邱�Ƃ�������܂����i�}1�A������2�Ԗڂ�3�Ԗڂ̃p�l���j�B���̑�2�̌����ꏊ�ł́AYEATS�h���C���̑a���I�ȕ��q�\�ʂ̂��ڂ݁iH3NT�|�P�b�g�Ɩ����j��H3�e�C����N���[1�`3�Ԗڂ܂ł�3�c���F�����Ă��邱�Ƃ�������܂����i�}1�A�E�[�̃p�l���j�B
�@X�������\����͂ł́A�^���p�N�����������i�ő̉��j���ĉ�͂��邽�߁A����ꂽ�\���������I�ȏf���Ă��Ȃ��\��������܂��B����̉�͂ł��A���GAS41�^���p�N���ɓ�̃q�X�g��H3�^���p�N�����������Ă���\���������Ă���A���ꂪ���ۂɐ��n�t����זE���̎p�ł��邩��������K�v������܂����B�����Ŏ��ɁANMR�@[11]�ɂ��GAS41��YEATS�h���C�������n�t���łǂ̂悤�Ƀq�X�g��H3�e�C���Ƒ��ݍ�p����̂��ׂ܂����B���̌��ʁA�q�X�g��H3�e�C����14�Ԗڂ̃��V���iK14ac�j��27�Ԗڂ̃��V���iK27ac�j���A�Z�`��������Ă���ƁAGAS41��YEATS�h���C���͖F�����P�[�W��H3NT�|�P�b�g�̊ԂɈʒu����A�~�m�_�i115�Ԗڂ̃`���V���c��FY115�j�����H3�y�v�`�h�Ƒ��ݍ�p���邱�Ƃ�������܂����i�}2�j�B
�@���̌��ʂ���AGAS41��YEATS�h���C���́A���n�t���ł�1�{��H3�e�C����2�J���̈قȂ镔�ʂ�2�J���̃|�P�b�g����ē����ɔF������2���F�����f������������܂����B�܂��AH3NT�|�P�b�g��ψق������^���p�N����|�{�זE�Ŕ���������������s�������ʂ�����A�����\���Ŋώ@���ꂽGAS41��H3NT�|�P�b�g�ƃq�X�g��H3��N���[�Ƃ̑��ݍ�p���זE���ł��N���Ă��邱�Ƃ���������܂����i�}3A�j�B
[�摜3]https://user.pr-automation.jp/simg/1706/77803/600_280_20231016130225652cb5d150e85.jpg
�}2�@���n�t����GAS41���q�X�g��H3��N���[�e�C���Ƒ��ݍ�p���镔��
�iA�j�n�tNMR�ɂ��GAS41��YEATS�h���C���̎c��̉��w�V�t�g�̔�r�B���C��H3�y�v�`�h�i��j�AK14�A�Z�`����H3�y�v�`�h�i���j
�@�@�@K27�@�A�Z�`����H3�y�v�`�h�i���j�̓H��O��ł̃V�O�i���̕ω��������BY����CSD�͉��w�V�t�g�̍����������BCSD���傫��
�@�@�@�ω����Ă���A�~�m�_�c��́A�H�肵�����ꂼ���H3�y�v�`�h�Ƃ̑��ݍ�p���������Ƃ������Ă���BX���ɕ��s��2��ނ̔j����
�@�@�@���ݍ�p�̗L�Ӎ������肷���ł���A�オ���ϒl��2�W�����A�������ϒl��1�W�������������l�������B�e�f�[�^�̉E����
�@�@�@���ꂼ��̃y�v�`�h�ƗL�ӂɑ��ݍ�p�����c���GAS41��YEATS�h���C���̕\�ʂɐF�Ń}�b�s���O���A�c��ԍ������x���Ŏ������B
�@�@�@�F�����P�[�W�̈ʒu�͎��F�̊ۈ�ŁAH3NT�|�P�b�g�̈ʒu�͔��F�̊ۈ�Ŏ����B
�iB�jGAS41��YEATS�h���C���\�ʂ̍\���ɂ�����115�Ԗڂ̃`���V���c��̈ʒu�i���F�j�B2�{��K14�A�Z�`����H3�y�v�`�h�̎��ۂ̍\��
�@�@�i���F�̎����j�͖͎��I�ɓ_���Ō���Ă���B�F�����P�[�W�Ɍ�������H3�y�v�`�h��12�Ԗڂ̃O���V���c��iH3G12�j�ƁAH3NT�|
�@�@�@�P�b�g�Ɍ�������H3�y�v�`�h��3�Ԗڂ̃X���I�j���c��iH3T3�j�̈ʒu�����x���Ŏ����BA�̉�͂ɂ����āAH3�y�v�`�h���A�Z�`����
�@�@�@����Ă���ƁA�����̎c��̊ԂɈʒu����115�Ԗڂ̃`���V���c��iY115�j�ɗL�ӂȉ��w�V�t�g�ω������o���ꂽ���Ƃ���A���n�t��
�@�@�@�ł�GAS41��YEATS�h���C����1�{��H3�e�C����2�J���̈قȂ�|�P�b�g�Łi=2���Łj�F�����邱�Ƃ��������ꂽ�B
[�摜4]https://user.pr-automation.jp/simg/1706/77803/600_452_20231016130229652cb5d5869cf.jpg
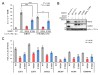
�}3�@GAS41�ɂ��q�X�g��H3��N���[�F���͍זE���@�\�ɏd�v
�iA�jGAS41�ƃq�X�g��H3�Ƃ̍זE���ł̌����]���B�זE����GAS41�̖쐶�^�iWT�j�܂���2��ނ̋@�\�ψّ́iW93A�܂���E109A�j�ƁA
�@�@�@�S���̃q�X�g��H3�܂���N���[�F���̈Ӌ`�ׂ邽�߂�1�Ԗڂ̃A���j���c��iA1�j�����������q�X�g��H3�������A�זE����2
�@�@�@��ނ̃^���p�N���Ԃ̑��ݍ�p�����o���鑪����@�ł���NanoBiT�A�b�Z�C�Ōu�����x�iY���̃��V�t�F���[�[�����j�𑪒肵���B
�@�@�@W93A��YEATS�h���C���̖F�����P�[�W�̋@�\�ψّ́AE109A��YEATS�h���C����H3NT�|�P�b�g�̋@�\�ψّ̂�GAS41�����ꂼ��
�@�@�@�����B�f�[�^��3��̓Ɨ������̕���±�W���덷�BHolm����ɂ�铝�v�I�L�Ӑ���*�܂���***�Ŏ����B
�iB�j�쐶�^�܂��͕ψّ̂�GAS41������GAS41�����}���זE�ɂ�����GAS41��H2A.Z�^���p�N���̖Ɖu�u���b�g��́BshCntl�͑Ώ�
�@�@�@�����AshGAS41��GAS41���}�����������i+�͏����A-�͖������j�������B�@�\�ψّ̂ɂ����Ă�GAS41�̃v���b�g�̔Z���ɑ�
�@�@�@����H2A.Z�̃v���b�g�̔Z���̔䂪�Ⴍ�Ȃ��Ă���AH2A.Z�^���p�N���̗ʂ��������Ă��邱�Ƃ�������B
�iC�j�쐶�^�܂��͕ψٌ^��GAS41������GAS41�����}���זE�ɂ�����GAS41�W�I��`�q�v�����[�^�[�ł̃N���}�`���Ɖu���~-���
�@�@�@���A���^�C��PCR�iChIP-qPCR�j�̉�͌��ʁB�N���}�`���Ɖu���~�iChIP�j�́A�זE�̃N���}�`����f�Љ����A����̍R�̂��F������
�@�@�@�^���p�N���₻�̉��w�C���̏�Ԃ��܂ރN���}�`���f�Ђ��擾������@�B��ʃ��A���^�C��PCR�iqPCR�j�́A���肷�鎎���Ɋ܂܂��
�@�@�@DNA�̗ʂ̐��肪�\��DNA�̑����@�B����2��ނ̎�@��g�ݍ��킹�邱�ƂŁA�N���}�`���̓���̗̈�Ɋ܂܂�Ă���^���p�N����
�@�@�@���̏C����Ԃ̗ʁi�N���}�`���ɂ������L���j�𑪒�ł���B����ChIP-qPCR��͂ł́A�q�X�g��H2A.Z�^���p�N���̐�L�����R��
�@�@�@�Ō��o�����B�eGAS41�W�I��`�q�������Ɏ������B�f�[�^��3��̓Ɨ������̕���±�W�����BWelch�̗���t����ɂ�铝�v�I�L�Ӑ�
�@�@�@��*�܂���**�Ŏ����B
�@GAS41�̋@�\�Ƃ��āA�k�N���I�\�[���Ƀq�X�g���̕ώ�^���p�N���ł���H2A.Z�^���p�N���̓����𑣐i���邱�ƂŁA����̈�`�q��]�ʂ��₷�����邱�Ƃ��m���Ă��܂��B�����Ŏ��ɁAGAS41�ƃq�X�g��H3�Ƃ̑��ݍ�p��GAS41�̍זE�@�\�ɕK�v���ǂ������m�F���邽�߂ɁAGAS41�ɂ��H2A.Z�^���p�N���̗ʓI�Ȑ���ɑ���e���ׂ܂����BGAS41�̈�`�q�����}���ɂ����H2A.Z�̗ʂ��������Ă���זE��p���āA�쐶�^GAS41�AH3NT�|�P�b�g���邢�͖F�����P�[�W��ψق�����GAS41�����������ʁA�ψّ̂������זE�ł�H2A.Z�^���p�N���̗ʂ��������邱�Ƃ�������܂����i�}3B�j�B�]���āAGAS41��H3NT�|�P�b�g�ƖF�����P�[�W�́A�זE����H2A.Z�^���p�N���̗ʂ��ێ����邽�߂ɏd�v�Ȃ��Ƃ�������܂����B
�@GAS41�̓N���}�`���̍\���𐧌䂷��^���p�N�������̂̍\�������̈�ł���A����̈�`�q�v�����[�^�[[12]�̈�̃k�N���I�\�[����H2A.Z�̓����𑣐i���邱�ƂŃN���}�`���̍\����ω������A���̈�`�q�̓]�ʂ����������܂��B�����ōŌ�ɁAGAS41���W�I�Ƃ��Ă����`�q�v�����[�^�[���H2A.Z�̃N���}�`���ɂ������L���ׂ܂����i�}3C�j�B����܂Œm���Ă���6��ނ̈�`�q�v�����[�^�[��GAS41�̕W�I�Ƃ��đI�����AGAS41�̖쐶�^�A�܂���H3NT�|�P�b�g���邢�͖F�����P�[�W�̕ψّ̂��זE�ɔ������Ă����̈�`�q�v�����[�^�[�Ɍ�������q�X�g��H2A.Z�̗ʂ��������܂����B���̌��ʁA�����6��ނ̈�`�q�v�����[�^�[�̂��ׂĂɂ����āA���ꂼ��̕ψّ̂�����זE�ł�H2A.Z�̃N���}�`���ɂ������L�����L�ӂɒቺ���܂����B�����̌��ʂ���AGAS41�͖F�����P�[�W����ăq�X�g��H3�̃A�Z�`������Ԃ�F�����邾���łȂ��AH3NT�|�P�b�g����ăq�X�g��H3��N���[��F�����邱�Ƃɂ��A�W�I�Ƃ����`�q�̃v�����[�^�[���ɔF�����A���̈�`�q�̓]�ʂ̊������Ɋ�^����d�g�݂���������܂����i�}4�j�B
[�摜5]https://user.pr-automation.jp/simg/1706/77803/600_207_20231016130231652cb5d7afc37.jpg
�}4�@GAS41�ɂ��G�s�Q�m������̎d�g�݂Ƒn��ւ̉��p
���}�́AGAS41�ɂ��G�s�Q�m������̎d�g�݂�͎��I�Ɏ����BGAS41��SRCAP�܂���Tip60/p400�ƌĂ��^���p�N�������̂��\������^���p�N���ł���A�k�N���I�\�[�����\������q�X�g��H3��N���[�e�C����N���[�iNT�Ŏ����j��K14ac�܂���K27ac�iKac�Ŏ����j���ɔF������B����ɂ��AGAS41��2�ʑ̂��܂�SRCAP�����̂܂���Tip60/p400�����͓̂���̈�`�q�v�����[�^�[�̃k�N���I�\�[���̃A�Z�`������Ԃ𐳂����F�����A���̃k�N���I�\�[���Ƀq�X�g��H2A.Z�𑣐i�I�ɓ������邱�Ƃœ���̈�`�q�̓]�ʊJ�n����������������ƍl������B�E�}�́A����������GAS41��H3NT�|�P�b�g�̍\����R���䕪�q�̍����I�ȊJ���Ɏ�����C���[�W�������B
����̊���
�@�����̂���זE�≊�ǍזE�ȂǂŃq�X�g���̃A�Z�`������Ԃُ̈킪�����邱�Ƃ���A�q�X�g���E�A�Z�`�����y�f�ɑ���j�Q�܂͓���̂���ɑ��鎡�Ö�Ƃ��Ď��p������Ă��܂��B�q�X�g���̃A�Z�`�����F����j�Q���鉻�����ɂ��Ă��A�u�����h���C���ɑ���j�Q�܂͐e�a����I�𐫂ɗD�ꂽ�������������J������A�������̂����ɑ���Տ��������i�s���ł��B���̈���AYEATS�h���C���ɑ���j�Q�܂̓u�����h���C���j�Q�܂قNJJ�����i��ł��炸�A����GAS41�ɑ���j�Q�܂̊J���͒x��Ă���ł��B
�@����̌����ɂ��AGAS41��YEATS�h���C���ɂ́A���̃^���p�N����YEATS�h���C���ɂ͌����Ȃ��@�\�I�ȃ|�P�b�g�����݂��邱�Ƃ�������܂����BGAS41�̔������P���זE�����łȂ��A�݂���זE��x����זE�Ȃǂɂ����Ă��ُ킪���邱�Ƃ��m���Ă��܂��B����A���炩�ɂȂ����\���������p���邱�ƂŁA����Ɍ�����GAS41��I��I�ɑj�Q���鉻�����������I�ɊJ�����邱�Ƃ����҂���܂��B
�_�����
���^�C�g����
GAS41 promotes H2A.Z deposition through recognition of the N terminus of histone H3 by the YEATS domain
�����Җ���
Masaki Kikuchi, Shohei Takase, Tsuyoshi Konuma, Kota Noritsugu, Saaya Sekine, Takahisa Ikegami, Akihiro Ito, and Takashi Umehara*
���G����
Proceedings of the National Academy of Sciences of the United States of America�iPNAS�j
��DOI��
https://doi.org/10.1073/pnas.2304103120
�⑫����
[1] GAS41�AYEATS�h���C��
GAS41�i�P���i����������j�����z��41�j�́A�q�X�g��H3��N���[�e�C���̉��w�C����F������^���p�N���ł���A�q�g�ł͑S����227�A�~�m�_���琬��B���q����YEATS�h���C���ƃR�C���h�E�R�C���h���C���ƌĂ��2��ނ̃h���C�������BYEATS�h���C����120�`140�A�~�m�_�ō\�������\�������h���C���ł���A�q�X�g���̃��V���c��̃A�Z�`�����C����A�V�����C����F��������������B�R�C���h�E�R�C���h���C���̓R�C���h�E�R�C���h���C�����m�ł̑��ݍ�p����ă^���p�N����2�ʑ̂��`��������������B
[2] �㐬��`���A�G�s�Q�m��
�זE����DNA�ɂ͈�`�����z��Ƃ��ċL�^����Ă���B�זE�ɂ́ADNA�̉���z��ȊO�ɂ��זE�̌����L������X�̏���݂��Ă���A������DNA��q�X�g���Ȃǂɑ��鉻�w�C���Ƃ��ċL�^����Ă���B����DNA�̎��ӂɋL�^�����DNA�̉���z��ȊO�̐��������㐬��`���i�G�s�W�F�l�e�B�b�N���j�ƌĂԁB�u�Q�m���v���זE���̑S�Ă�DNA�̉���z��Ƃ��ċL�^���ꂽ��`���̑��̂��w���̂ɑ��A�u�G�s�Q�m���v��DNA��q�X�g���Ȃǂ̉��w�C���ɂ���čזE�̌����L����������܂߂����̂��w���B
[3] �q�X�g��H3�^���p�N���̃A�Z�`�����C��
�q�X�g���ƌĂ��^���p�N����DNA�������t���邱�ƂŒ����DNA���j���ɔ[�߂���������B�q�X�g����DNA�������t���邽�߂ɁA�q�X�g��H3��H4��2���W�܂���H3-H4�l�ʑ̈�ƃq�X�g��H2A��H2B��1���W�܂���H2A-H2B��ʑ̓���琬��q�X�g�����ʑ̂��`�����Ă���B�q�X�g���͐�����Ԃ��č����ۑ�����Ă���A����̃A�~�m�_�c����w�C������Ă���Ⴊ�������m���Ă���B��\�I�ȉ��w�C���ł���A�Z�`�����C���̏ꍇ�A�^���p�N���̃��V���c��̑����A�~���ɃA�Z�`����iCH3CO−�j����������B�q�X�g��H3�̏ꍇ�AN���[����1�c��ڂ��琔����4�ԖځA9�ԖځA14�ԖځA18�ԖځA23�ԖځA27�ԖځA36�ԖڂȂǂ̃��V���c��A�Z�`�����y�f�ɂ���ăA�Z�`��������A���̂����̑����͈�`�q�]�ʂ̊�������ԂƑ��ւ��Ă���B
[4] �^�j�זE
�^�j�זE�͊j���ŕ�܂ꂽ�j�₻�̑��̏��튯�����זE�̂��ƁB�^�j�זE�̃Q�m��DNA�́A�k�N���I�\�[������{�P�ʂƂ���Ïk�����\�����`�����āA�זE�����̑啔�����߂�Ԋ��ɂ����Ă͍זE�j�̒��Ɏ��[���ꂽ��Ԃő��݂���B�^�j�זE�ō\�������^�j�����̑�\�I�Ȑ����Ƃ��Ă͒P�זE�ō\�������y���A���זE�ō\������鍩����}�E�X�A�q�g�Ȃǂ���������B
[5] �k�N���I�\�[���A�N���}�`��
�^�j�זE�j����DNA�ƃq�X�g�����ʑ́iH2A�AH2B�AH3�AH4�̃^���p�N����2���܂ޕ����́j�������I�Ɋ����t���Č`�����ꂽ�����̂��k�N���I�\�[���ƌĂԁB�k�N���I�\�[���̒��S������145�`147�����DNA���q�X�g�����ʑ̂Ɋ����t�����R�A���q���琬��B������DNA�ƕ����̃k�N���I�\�[���ō\������鐔���̍\���̂̓N���}�`���ƌĂ��B
[6] �]��
��`�qDNA�̉���z���RNA�|�������[�[���ǂݎ��A2�{��DNA�̕Е��̉���z��ɑΉ�����RNA���������锽�����u�]�ʁv�ƌĂԁBRNA�|�������[�[�́ADNA�𒒌^�Ƃ���RNA���\�������{�P�ʂ̃��{�k�N���I�`�h���d������y�f�ł���A���j�����ł�1��ނ�RNA�|�������[�[�A�^�j�����ł�RNA�|�������[�[�T�A�U�A�V��3��ނ����݂���B�����̈�`�q�͂��̖{�̕��������ł͓]�ʂ��N���炸�ɁA��`�q�̏㗬�܂��͉����ɓ]�ʔ��������I�E�ʓI�ɕω�������DNA�z�K�v�ł���B�����͂��̈ʒu��@�\�ɉ����ăv�����[�^�[��G���n���T�[�ƌĂ��B
[7] N���[
�^���p�N���̓A�~�m�_�c�������ɘA�������|���y�v�`�h�ō\������邱�Ƃ���A���̎n�܂�ƏI��肪����B�^���p�N���̎n�܂�ƂȂ�1�Ԗڂ̎c��i�܂��͂��̎卽�A�~�m��j��N���[�A�I���ƂȂ�Ō�̎c��i�܂��͂��̎卽�J���{�L�V����j��C���[�ƌĂ��B�^���p�N���ɂ���Ă�N���[�c��̃A�~�m��͍זE���ŃA�Z�`�����C�����Ă��邪�A�q�X�g��H3��N���[�c��̃A�~�m��͉��w�C�����Ă��Ȃ��B�܂��A�q�X�g����N���[�c��ɑ������\�c��̗̈�͓���̍\���������Ȃ��e�C���i�����j�Ƃ��Đ��n�t���ŗh�炢�ł���B�q�X�g��N���[�e�C���̃��V���c����̃A�~�m��́A�A�Z�`������`�����Ȃǂ̉��w�C�����₷���A���̓���̏C����Ԃ͈�`�q�����̊�������}�����̏�ԂƑ��ւ��Ă���B
[8] ���V���c��
�^���p�N�����\������A�~�m�_�̈�B1�������̂�K�B�����ɃA�~�m��������߁A�^���p�N�����̎c��Ƃ��ăA�~�m��ւ̃A�Z�`������`�����C���̕W�I�ƂȂ�B
[9] �u�����h���C��
110�`120�A�~�m�_���琬��^���p�N���̐܂��ݍ\���B���̐܂��ݍ\���̒��S�����ɂ��ڂ݂������A���̂��ڂ݂���ăq�X�g����N���[�e�C���Ȃǂɑ��݂��郊�V���c��̃A�Z�`������Ԃ���ٓI�ɔF���ł���B
[10] �P���i����������j�זE
�]���ɐ����鈫���x��������ᇂ̈��B
[11] NMR�@
���q�i�^���p�N���Ȃǁj�ɑ��č�����̊����œd���g���Ǝ˂��A���q���\�����錴�q�̂��ꂼ�ꌴ�q�j�����ӂ̉��w�I���ɉ����ē���̓d���g���z�����鋤���ۂ��ϑ����邱�Ƃŕ��q�̗��̍\���₻�̕ω��𐄒肷���@�B���q�j�̎�ނ������ł����q�j�̎��ӊ��̈Ⴂ�ɂ���ċ����g���͕ω����A���w�V�t�g�ƌĂ�镪�q�̗��̍\���Ɋւ���������B
[12] ��`�q�v�����[�^�[
DNA��ň�`�q�iRNA�j�̓]�ʂ��J�n�����ʒu�̋߂��ɂ���A��`�q��������@�\��������z��B��`�q�v�����[�^�[�ɐ������̊�{�]�ʈ��q��RNA�|�������[�[���������邱�ƂŁA����̈�`�q���]�ʂ����ʒu��]�ʂ����ʂ����܂�ƍl�����Ă���B
���������O���[�v
�����w������
�@�����@�\�Ȋw�����Z���^�[
�@�G�s�W�F�l�e�B�N�X���䌤���`�[���i���������j
�@�`�[�����[�_�[�i���������j�@�@�@ �@�~�����j�@�i�E���n���E�^�J�V�j
�@�@�@�i���@�n��^���p�N����͊�Ճ��j�b�g�@�㋉�������j
�@�@�@�������i���������j�@�@�@�@�@�@�@ �@�e�n�����@�i�L�N�`�E�}�T�L�j
�i���@������Ȋw�����Z���^�[�@�Ɖu�튯�`�������`�[���@�������j
�������Ȋw�����Z���^�[
�@�P�~�J���Q�m�~�N�X�����O���[�v
�@�@�q����nj������@�@�@�@�@�@�@�@�@�@�ɓ������@�i�C�g�E�E�A�L�q���j
�@�@�i������ȑ�w�@�����Ȋw���@�����j
������ȑ�w
�@�����Ȋw���@�זE���Ȋw������
�@�@���ʌ������iPD�j �i���������j�@ �@�����ĕ��@�i�^�J�Z�E�V���E�w�C�j
�@�@������ �@�����P���@�i�m���c�O�E�R�E�^�j
�@�@�C�m�ے��Q�N���i���������j�@ �@�֍���ʁ@�i�Z�L�l�E�T�A���j
���l�s����w
�@��w�@������Ȋw�����ȁ@�\���G�s�Q�m���Ȋw������
�@�@���� �@�����@���@�i�R�k�}�E�c���V�j
�@�@���� �@�r��M�v�@�i�C�P�K�~�E�^�J�q�T�j
�����x��
�{�����́A�����w�������^�c���t���i�����@�\�Ȋw�����j�Ŏ��{���A�Ȋw�Z�p�U���@�\�iJST�j�헪�I�n���������i���ƌl�^�����iPRESTO�A���������j�u�זE�@�\�̍\���I�ȗ����Ɛ���i�����̈摍���F��c�ȁj�v�̌����ۑ�u�w�G�s�k�N���I�\�[���x�̐����ȍč\���ɂ���`�q���������́i������\�ҁF�~�����j�j�v�A���{�w�p�U����iJSPS�j�Ȋw����������Ɗw�p�ϊv�̈挤���iA�j�uDNA�̕������痝������Q�m�����_���e�B�i�̈��\�ҁF���R���q�j�v�A����Ռ����iB�j�u����זE�Ŋ拭�Ɉێ�����钴�A�Z�`�����G�s�Q�m���𑀍삷��i������\�ҁF�~�����j�j�v�A����茤���uGAS41�ɂ��A�Z�`�����k�N���I�\�[���F���@�\�̉𖾁i������\�ҁF�e�n�����j�v�Ȃǂɂ�鏕�����čs���܂����B